Kierownik grupy
dr hab. n. med. Magdalena Czeredys - tel. 22 60 86 540, Ten adres pocztowy jest chroniony przed spamowaniem. Aby go zobaczyć, konieczne jest włączenie w przeglądarce obsługi JavaScript. pokój nr 602
Doktoranci
mgr Victoria Graffe Pereira - tel. 22 60 85 41, Ten adres pocztowy jest chroniony przed spamowaniem. Aby go zobaczyć, konieczne jest włączenie w przeglądarce obsługi JavaScript. ; pokój nr 602
mgr Mahadi Hassan Fahim - tel. 22 60 85 41, Ten adres pocztowy jest chroniony przed spamowaniem. Aby go zobaczyć, konieczne jest włączenie w przeglądarce obsługi JavaScript. ; pokój nr 602
mgr Hathiringe Dona Sandali Kavishka - tel. 22 608 85 41, Ten adres pocztowy jest chroniony przed spamowaniem. Aby go zobaczyć, konieczne jest włączenie w przeglądarce obsługi JavaScript.

Tematyka badawcza
Prowadzone badania mają na celu zrozumienie mechanizmów choroby Huntingtona oraz opracowywanie potencjalnych strategii terapeutycznych z użyciem ludzkich indukowanych komórek macierzystych (hiPSC).
Główne zagadnienia badawcze naszej grupy dotyczą:
- zrozumienia neurodegeneracyjnego i neurorozwojowego podłoża choroby Huntingtona
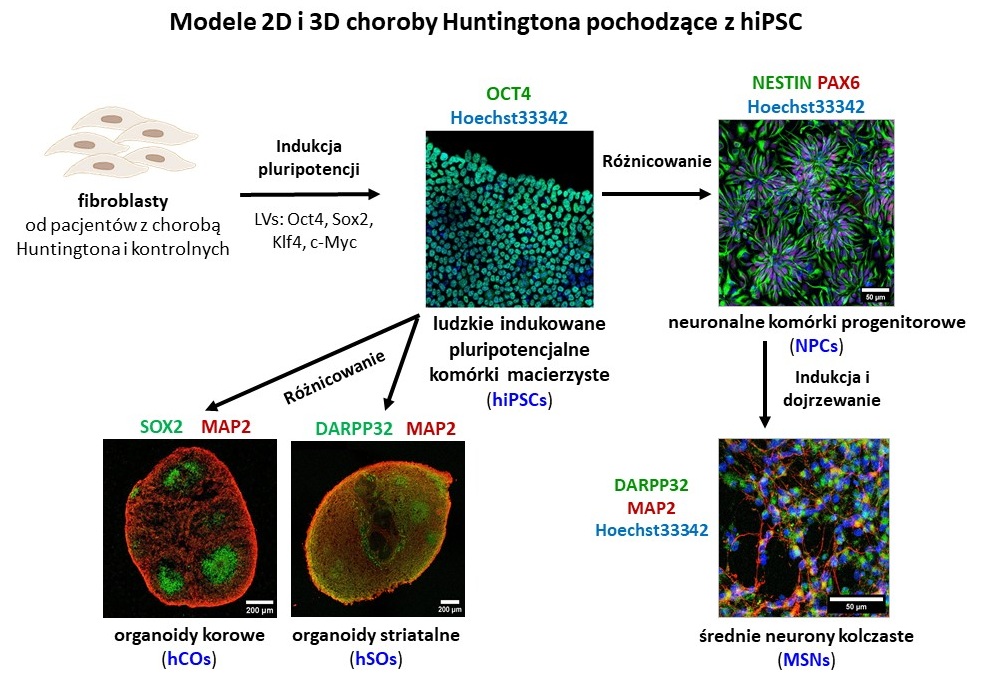
- uzyskiwania modeli choroby Huntingtona pochodzących z hiPSC
- modelowania choroby Huntingtona z wykorzystaniem zróżnicowanych z hiPSC neuroprogenitorów (NPC) i neuronów MSNs (modele 2D), organoidów oraz assembloidów (modele 3D)
- identyfikacji celów terapeutycznych w chorobie Huntingtona przy użyciu powyższych modeli
- modelowania choroby Huntingtona z wykorzystaniem bezpośredniego reprogramowania neuronów (indukowane neurony, iN)
- zrozumienia mechanizmów choroby Huntingtona z użyciem analiz multiomicznych
- testowania metod terapeutycznych (leków, edycji genomu) w modelach in vitro choroby Huntingtona (NPC, neuronów, organoidów)
Granty
Projekty realizowane:
- “Assembloidy korowo-striatalne pochodzące z ludzkich iPSCs jako nowy model do badań zaburzeń neurorozwojowych wywoływanych przez zmutowaną huntingtynę” NCN OPUS, nr. 2023/49/B/NZ3/04131, 2024 – 2028; kierownik projektu: dr hab. Magdalena Czeredys
- “Innowacyjna platforma modelowania organoidów i testowania terapii w ludzkich chorobach neurologicznych i onkologicznych” nr. KPOD.07.07-IW.07-0105/24, 2024 – 2025; kierownik projektu: dr hab. Dawid Walerych, współpraca naukowa/konsultant: dr hab. Magdalena Czeredys
- “Odkrycie roli Nrf2 w patofizjologii niedoboru fosfomannomutazy 2” GACR nr. 22-18235S, 2022 – 2025; kierownik projektu: prof. Hana Hansikova i dr Nina Ondruskova, Współpraca naukowa/wykonawca: dr hab. Magdalena Czeredys
- “Molekularne przyczyny genetyczne i biochemiczne konsekwencje wrodzonych zaburzeń glikozylacji” AZV CR NU22-07-00474, 2022 – 2025; kierownik projektu: prof. Hana Hansikova, Współpraca naukowa: dr hab. Magdalena Czeredys
Projekty zakończone:
- “Powiązanie zaburzonej sygnalizacji Ca2+ i UPR z patologią choroby Huntingtona w modelu mysim YAC128 oraz w neuronach od pacjentów z HD uzyskanych w wyniku różnicowania iPSC” OPUS NCN nr. 2019/33/B/NZ3/02889; 2020 – 2024; kierownik projektu: dr hab. Magdalena Czeredys
- “Rola białka CacyBP/SIP w zaburzeniu ubikwitynacji beta-kateniny u myszy YAC128, modelu choroby Huntingtona” NCN SONATA nr. 2014/15/D/NZ3/05181; SONATA 8, 2015-2019; kierownik projektu: dr hab. Magdalena Czeredys
- “Huntingtin-associated Protein 1 aktywuje pojemnościowy napływ wapnia poprzez aktywację receptorów IP3 w chorobie Huntingtona” FNP BRIDGE, nr. POMOST/2013-8/4/0193 2014 – 2015; kierownik projektu: dr hab. Magdalena Czeredys
- “Pojemnościowy napływ wapnia (SOCE) jako nowy cel terapeutyczny w chorobach neurodegeneracyjnych”. Polsko-Nimiecko-Rosyjski Grant EU ERA.Net RUS, NCBR nr. NCBR/ERA.Net RUS/03/2012, 2012 – 2014; wykonawca: dr hab. Magdalena Czeredys
Współpraca:
krajowa
- prof. dr hab. Marta Olejniczak; Zakład Inżynierii Genomowej, Instytut Chemii Bioorganicznej, Polskiej Akademii Nauk
- dr. hab. Stanisław Dunin-Horkawicz, Laboratorium Bioinformatyki Strukturalnej, Centrum Badań Biologiczno-Chemicznych Uniwersytetu Warszawskiego
międzynarodowa
-
Dr. Karolina Pircs and Dr. Attila Szücs, Neurobiology and Neurodegenerative Diseases Group, Institute of Translational Medicine, Semmelweis University
-
In-Hyun Park, Yale Stem Cell Center
-
Gabriel Balmus, UK Dementia Research Institute, University of Cambridge
-
Hana Hansikova, Laboratory for Study of Mitochondrial Disorders, Department of Pediatric and Adolescent Medicine, Charles University in Prague
-
Jiri Klempir, Department of Neurology, Centre of Clinical Neuroscience and Institute of Anatomy, Charles University in Prague
-
Georg Bernhard Landwehrmeyer, Department of Neurology, University of Ulm
-
Alzbeta Mühlbäck, Department of Neurology, University of Ulm, Isar-Amper-Klinikum, Huntington-Zentrum-Süd, Klinik Taufkirchen
-
Katsuhiko Mikoshiba, Lab for Cell Calcium Signaling, Shanghai Institute for Immunochemical Studies (SIAIS), ShanghaiTech University
Metody badawcze
- zaawansowane techniki hodowli komórkowych oparte o hiPSC: wyprowadzanie linii hiPSC z fibroblastów od pacjentów i osób kontrolnych, charakterystyka linii hiPSC, uzyskiwanie hodowli NPC pochodzących z hiPSC, uzyskiwanie hodowli MSNs pochodzących z hiPSC (neurony prążkowia), hodowla organoidów striatalnych i korowych pochodzących z hiPSC, otrzymywanie asembloidów korowo-striatalnych, wzbogacanie organoidów w komórki mikrogleju
- uzyskiwanie reprogramowanych bezpośrednio neuronów (iN)
- edycja genomu linii hiPSC przy użyciu CRISPR-Cas9
- hodowle pierwotne neuronów i astrocytów z myszy i szczurów
- uzyskiwanie i hodowla komórek macierzystych miazgi zębowej (DPSC)
- produkcja lentiwirusów
- metody biologii molekularnej i biochemii
- obrazowanie odpowiedzi wapniowej w pojedynczej komórce
- badania przesiewowe leków
- techniki mikroskopowe: obrazowanie przyżyciowe, immunocytochemia; cytometria przepływowa, sekwencjonowanie RNA
- modele zwierzęce: myszy YAC128 (transgeniczny mysi model choroby Huntingtona)
Aparatura
- laminar do hodowli komórek ESCO Class II BSC
- inkubatory do hodowli komórek (CO2 MCO-171AICUVD, Heal Force Smart Cell)
- wytrząsarka do hodowli organoidów Thermo Scientific
- łaźnia wodna
- mikroskop fluorescencyjny ZEISS Axiovert 5 z kamerą Axiocam
- automatyczny licznik komórek LUNA II
- termocykler Eppendorf
- dewar ANTECH do przechowywania linii komórkowych w ciekłym azocie
- wirówki laboratoryjne (Jouan CR3, M-Universal MPW, Eppendrorf)
Wybrane publikacje
* autor korespondencyjny
- Piechota M, Latoszek E, Liszewska E, Hansíková H, Klempíř J, Mühlbäck A, Landwehrmeyer GB, Kuźnicki J, Czeredys M*. Generation of two human iPSC lines from dermal fibroblasts of adult- and juvenile-onset Huntington's disease patients and two healthy donors. Stem Cell Res. 2023 Sep;71:103194. doi: 10.1016/j.scr.2023.103194.
- Latoszek E, Piechota M, Liszewska E, Hansíková H, Klempíř J, Mühlbäck A, Landwehrmeyer GB, Kuznicki J, Czeredys M*. Generation of three human iPSC lines from patients with Huntington's disease with different CAG lengths and human control iPSC line from a healthy donor. Stem Cell Res. 2022 Oct;64:102931. doi: 10.1016/j.scr.2022.102931.
- Markowska-Barkic A, Lewicka E, Czeredys M, Mitura M, Jagura-Burdzy G*. Deciphering the Regulatory Circuits of RA3 Replication Module - Mechanisms of the Copy Number Control. Int J Mol Sci. 2022 Sep 1;23(17):9964. doi: 10.3390/ijms23179964.
- Latoszek E, Wiweger M, Ludwiczak J, Dunin-Horkawicz S, Kuznicki J*, Czeredys M*. Siah-1-interacting protein regulates mutated huntingtin protein aggregation in Huntington's disease models. Cell Biosci. 2022 Mar 19;12(1):34. doi: 10.1186/s13578-022-00755-0.
- Latoszek E, Czeredys M*. Molecular Components of Store-Operated Calcium Channels in the Regulation of Neural Stem Cell Physiology, Neurogenesis, and the Pathology of Huntington's Disease. Front Cell Dev Biol. 2021 Apr 1;9:657337. doi: 10.3389/fcell.2021.657337.
- Czeredys M*. Dysregulation of Neuronal Calcium Signaling via Store-Operated Channels in Huntington's Disease. Front Cell Dev Biol. 2020 Dec 23;8:611735. doi: 10.3389/fcell.2020.611735.
- Grzeczkowicz A, Gruszczynska-Biegala J, Czeredys M, Kwiatkowska A, Strawski M, Szklarczyk M, Koźbiał M, Kuźnicki J, Granicka LH*. Polyelectrolyte membrane scaffold sustains growth of neuronal cells. J Biomed Mater Res A. 2019 Apr;107(4):839-850. doi: 10.1002/jbm.a.36599.
- Czeredys M*, Vigont VA, Boeva VA, Mikoshiba K, Kaznacheyeva EV, Kuznicki J. Huntingtin-Associated Protein 1A Regulates Store-Operated Calcium Entry in Medium Spiny Neurons From Transgenic YAC128 Mice, a Model of Huntington's Disease. Front Cell Neurosci. 2018 Oct 26;12:381. doi: 10.3389/fncel.2018.00381.
- Czeredys M*, Maciag F, Methner A, Kuznicki J. Tetrahydrocarbazoles decrease elevated SOCE in medium spiny neurons from transgenic YAC128 mice, a model of Huntington's disease. Biochem Biophys Res Commun. 2017 Feb 19;483(4):1194-1205. doi: 10.1016/j.bbrc.2016.08.106.
- Czeredys M, Gruszczynska-Biegala J, Schacht T, Methner A, Kuznicki J*. Expression of genes encoding the calcium signalosome in cellular and transgenic models of Huntington's disease. Front Mol Neurosci. 2013 Nov 25;6:42. doi: 10.3389/fnmol.2013.00042.
- Czeredys M, Samluk Ł, Michalec K, Tułodziecka K, Skowronek K, Nałęcz KA*. Caveolin-1--a novel interacting partner of organic cation/carnitine transporter (Octn2): effect of protein kinase C on this interaction in rat astrocytes. PLoS One. 2013 Dec 13;8(12):e82105. doi: 10.1371/journal.pone.0082105. PMID: 24349196; PMCID: PMC3862573.
- Tułodziecka K, Czeredys M, Nałęcz KA*. Palmitoylcarnitine affects localization of growth associated protein GAP-43 in plasma membrane subdomains and its interaction with Gα(o) in neuroblastoma NB-2a cells. Neurochem Res. 2013 Mar;38(3):519-29. doi: 10.1007/s11064-012-0944-5. Epub 2012 Dec 9. Erratum in: Neurochem Res. 2013 Nov;38(11):2450-1.
- Samluk L, Czeredys M, Skowronek K, Nałęcz KA*. Protein kinase C regulates amino acid transporter ATB(0,+). Biochem Biophys Res Commun. 2012 May 25;422(1):64-9. doi: 10.1016/j.bbrc.2012.04.106.
- Samluk Ł, Czeredys M, Nałęcz KA*. Regulation of amino acid/carnitine transporter B 0,+ (ATB 0,+) in astrocytes by protein kinase C: independent effects on raft and non-raft transporter subpopulations. J Neurochem. 2010 Dec;115(6):1386-97. doi: 10.1111/j.1471-4159.2010.07040.x.
- Czeredys M, Mysiorek C, Kulikova N, Samluk Ł, Berezowski V, Cecchelli R, Nałecz KA*. A polarized localization of amino acid/carnitine transporter B(0,+) (ATB(0,+)) in the blood-brain barrier. Biochem Biophys Res Commun. 2008 Nov 14;376(2):267-70. doi: 10.1016/j.bbrc.2008.08.122.
- Kulinska A, Czeredys M, Hayes F, Jagura-Burdzy G*. Genomic and functional characterization of the modular broad-host-range RA3 plasmid, the archetype of the IncU group. Appl Environ Microbiol. 2008 Jul;74(13):4119-32. doi: 10.1128/AEM.00229-08.
- Miecz D, Januszewicz E, Czeredys M, Hinton BT, Berezowski V, Cecchelli R, Nałecz KA*. Localization of organic cation/carnitine transporter (OCTN2) in cells forming the blood-brain barrier. J Neurochem. 2008 Jan;104(1):113-23. doi: 10.1111/j.1471-4159.2007.05024.x.
- Nałecz KA*, Szczepankowska D, Czeredys M, Kulikova N, Grześkiewicz S. Palmitoylcarnitine regulates estrification of lipids and promotes palmitoylation of GAP-43. FEBS Lett. 2007 Aug 21;581(21):3950-4. doi: 10.1016/j.febslet.2007.07.027.






